روى المحامي حمد عيسى المناعي قصة واقعية لضحية من كبار السن خسرت مليون ريال بسبب الاحتيال الإلكتروني. وأشار المناعي – في مقابلة مع...
رئيس مجلس الإدارة : د. خالد بن ثاني آل ثاني

رئيس التحرير: جابر سالم الحرمي

مساحة إعلانية

وافقت هيئة الغذاء والدواء الأمريكية /FDA/، على دواء جديد لمكافحة السمنة، يعمل على خفض الوزن بنسبة 15%، في خطوة جديدة لمواجهة هذا الداء الذي يودى بحياة الكثيرين حول العالم ويسبب مضاعفات صحية خطيرة تتعلق بأمراض القلب والسرطان وارتفاع ضغط الدم. وأكدت الهيئة أن العقار الجديد يتكون من نسخة مركبة من هرمون الأمعاء الذي يحد من الشهية، ويقوم المرضى بحقنه أسبوعيًا تحت الجلد، مثل أدوية إنقاص الوزن الأخرى. وأوصت الدراسات بضرورة ممارسة التمارين الرياضية واتباع نظام غذائي صحي، عند تناول الدواء الجديد لخسارة الوزن بأمان. وذكر الخبراء أن الآثار الجانبية المحتملة لعقار السمنة الجديد، تتمثل مشاكل الجهاز الهضمي، بما في ذلك الغثيان والإسهال والقيء. وأوضحوا أيضا أن الدواء يحمل خطرا محتملا للإصابة بنوع من أورام الغدة الدرقية، لذلك لا ينبغي أن يتناوله الأشخاص الذين لديهم تاريخ شخصي أو عائلي من بعض أورام الغدة الدرقية والغدد الصماء. وأشار الخبراء إلى أن الدواء الجديد يعد نسخة حديثة بجرعة أعلى من أحد عقاقير السكري من النوع الثاني، والذى يعمل على التحكم في الوزن على المدى الطويل، بعد أن توصلت الدراسات التي أجريت على هذا العقار من خلال الاستعانة بعدد من المشاركين الذين تناولوه ونجحوا في فقدان 15% من الوزن، على مدار 14 شهرا، مقارنة بمشاركين آخرين حصلوا على عقاقير أخرى لكنهم لم يخسروا إلا 2.5% من أوزانهم فقط. وقال الدكتور هارولد بايز، المدير الطبي لمركز لويزفيل لأبحاث الأيض وتصلب الشرايين، إن الأدوية الحالية المنتشرة لمكافحة السمنة لم تتمكن من إنقاص أوزان مستخدميها بأكثر من 5 إلى 10 بالمائة. وأوضحت بيانات هيئة الغذاء والدواء الأمريكية أن هناك أكثر من 100 مليون بالغ يعانون من السمنة المفرطة في الولايات المتحدة. وأشارت الدراسات إلى أن فقدان 5 بالمائة من الوزن يمكن أن يجلب فوائد صحية مثل تحسين الطاقة وضغط الدم وسكر الدم ومستويات الكولسترول.
3969
| 06 يونيو 2021

منحت هيئة الغذاء والدواء الأمريكية FDA، ترخيصا، باستخدام الطوارئ، لجهاز التنفس الصناعي الذى طورته الإدارة الوطنية للملاحة الجوية والفضاء NASA، لعلاج المرضى الذين يعانون من فيروس كورونا( كوفيد-19) وذكر بيان لهيئة الغذاء والدواء الأمريكية، أنه تمت إضافة جهاز التنفس الصناعي إلى قائمة أجهزة التهوية المصرح بها وموصلات أنابيب جهاز التنفس الصناعي وملحقات جهاز التنفس الصناعي تحت جهاز التهوية EUA التي تم إصدارها، استجابة للمخاوف المتعلقة بعدم كفاية الإمداد وتوافر أجهزة التهوية التي تم تصفيتها من قِبل إدارة الأغذية والعقاقير، لاستخدامها في إعدادات الرعاية الصحية لعلاج المرضى أثناء جائحة فيروس كورونا. وقال مفوض هيئة الغذاء والدواء ستيفن إم هان إن مكافحة الفيروس وعلاج المرضى خلال هذا الوباء العالمي غير المسبوق يتطلب مناهج وإجراءات مبتكرة. وأضاف أن الهيئة قامت بتضمين جهاز NASA VITAL، المصمم خصيصًا للمرضى الذين يعانون من ( كوفيد- 19 )، من خلال توفير الدعم التنفسي للمرضى الذين يعانون من فشل تنفسي أو قصور.
1366
| 01 مايو 2020

حذّرت هيئة الغذاء والدواء الأمريكية (FDA) من تناول العجين الخام أو مزيج الكعك قبل خبزه أو طهيه، بسبب مخاطر الإصابة ببكتريا إي كولاي المعوية التي تصيب القولون تحديدا بسبب الدقيق. وأوضحت الهيئة في إفادة جديدة لها، اليوم الجمعة، أن تحذيراتها تأتي تأكيدا لتحذيرات سابقة من خطر تناول العجين الخام وخليط الكعك بسبب البيض النيئ الذي يشكل خطورة الإصابة بالسالمونيلا. وأصدرت الهيئة إرشادات لضمان سلامة الغذاء، نصحت بعدم تناول أي نوع من عجين البسكويت الخام وخليط الكعك وأي نوع آخر من العجين الخام قبل إخضاعه للطهي أو الخبز. ونصحت بغسل اليدين وأسطح الإعداد والأواني جيدا بعد عجن الدقيق أو منتجات العجين الخام، بالإضافة إلى عدم السماح للأطفال باللعب بالعجين المصنوع من دقيق خام. ووجهت الهيئة تحذيرا للمطاعم وباعة التجزئة بعدم تقديم عجين خام للزبائن أو تقديم عجائن للأطفال للعب بها، بالإضافة إلى فصل الغذاء النيئ عن الأغذية الأخرى أثناء إعدادها تفاديا لحدوث أي تلوث. وأوصت الهيئة باتباع إرشادات التعبئة لطهي المنتجات التي تحتوي على دقيق في درجات حرارة مناسبة لأوقات محددة، واتباع الإرشادات المدونة على العبوة لتبريد المنتجات التي تحتوي على عجين خام بعد الشراء مباشرة حتى موعد الخبز. وقالت ليزلي سموت، المستشارة البارزة في الهيئة، إن الدقيق بمفرده يشكل خطورة أيضا. وأضافت :الدقيق من مشتقات حبوب تأتي مباشرة من الحقل وليست معالجة لقتل البكتريا. ويمكن لبكتريا تأتي من نفايات الحيوانات في الحقل أن تلوث الحبوب التي يحصدونها بعد ذلك وتطحن في هيئة دقيق. وكان عشرات الأشخاص في شتى أرجاء الولايات المتحدة أصيبوا عام 2016 بإعياء نتيجة سلالة بكتيرية تتعلق بالدقيق. وتسبب بكتريا إي كولاي مغصا معويا وإسهالا ويتعافى المصاب في غضون أسبوع، وفي حالات نادرة تسبب البكتريا نوعا من الفشل الكلوي يطلق عليه اسم متلازمة انحلال الدم اليوريمي. ويكون صغار السن والمسنون وأولئك الذي يعانون من ضعف الجهاز المناعي الأكثر عرضة لخطر الإصابة بمضاعفات.
1911
| 08 ديسمبر 2017

وافقت هيئة الغذاء والدواء الأمريكية (FDA) على استخدام أول عقار "رقمي" في الولايات المتحدة، أي يمكن تتبعه رقميًا في الجسم، ويستخدم لعلاج مرض الفصام. وأوضحت الهيئة في بيان، اليوم الثلاثاء، أن العقار الجديد يحمل اسم "أبليفي" (Abilify) لعلاج مرض الفصام "الشيزوفرينيا" والهلوسة، بالإضافة لاستخدامه كعلاج إضافي لعلاج الاكتئاب لدى البالغين. وأضافت الهيئة أن هذا القرص من الدواء يحتوي على مستشعر قابل للهضم ينشط لدى تفاعله مع سوائل المعدة، فيسجل تناول المرضى للعقار. وبحسب الهيئة، فإن "القرص الجديد يرسل البيانات لأجهزة الهواتف الذكية للمرضى ليتيقنوا من تناولهم الدواء، وللأطباء أيضًا في حالة موافقة المرضى". وكانت الآثار الجانبية الأكثر شيوعًا للعقار، بحسب الهيئة، "هي الغثيان والقيء والإمساك والصداع والدوخة، بالإضافة إلي أنه قد يحدث تهيج الجلد في بعض المرضى". ووافقت الهيئة على العقار لأول مرة في عام 2002 لعلاج الفصام قبل أن يتحول لعقار رقمي، كما أجازت الهيئة نظام المستشعر القابل للهضم للتناول في الأسواق لأول مرة في عام 2012. والفصام هو اضطراب نفسي مزمن يصيب المخ، ويؤثر على طريقة تفكير وتصرُّف المريض، ويؤدي إلى ضعف الذاكرة، وفقدان التركيز، وضعف التفاعل الاجتماعي، والإدراك والسلوكيات الاستكشافية، وارتفاع مستويات القلق وعدم القدرة على تمييز المعلومات غير الضرورية.
5338
| 14 نوفمبر 2017

وافقت هيئة الغذاء والدواء الأمريكية (FDA) على اختبار جديد يتيح التشخيص السريع لحالات الحساسية باستخدام قطرة دم واحدة، وفي 8 دقائق فقط. الاختبار طورته شركة "أيبايونيك" السويسرية، التابعة للمعهد الاتحادي السويسري للتقنية في لوزان، واستغرق تطوير الاختبار 5 سنوات. وأوضحت الشركة، في بيان عبر موقعها الإلكتروني، أن الاختبار يتطلب كبسولات تستعمل لمرة واحدة، توضع في جهاز اختبار محمول يستطيع حاليًا اكتشاف مسببات الحساسية الشائعة الأربعة وهي الكلاب والقطط وغبار طلع الأشجار والعشب. وأضافت أن قطرة الدم توضع في جهاز الاختبار على طبق يشبه القرص المضغوط بعد خلطه مع كاشف كيميائي، وتظهر النتائج الأولية على شاشة عالية الدقة خلال 5 دقائق، وتحدد نوع الحساسية خلال 8 دقائق من إجراء الاختبار. ووفقًا للشركة، فإن الاختبار الذي يطلق عليه اسم "أيبايوسكوب" يعد أسرع اختبار حساسية في العالم، إذ بات بالإمكان اكتشاف مسببات الحساسية الأربعة الأكثر شيوعًا دون الاستعانة بالاختبارات التقليدية، بالإضافة لسهولة إجراء الاختبار، وسرعة ظهور النتائج. وقال نيكولاس دوراند، المدير التنفيذي لشركة أيبايونيك "يعاني نحو 25 مليون شخص بالغ في الولايات المتحدة الأمريكية من التهاب الأنف التحسسي، وما زال الرقم في تزايد". وأضاف أن تسجيل الاختبار لدى هيئة الغذاء والدواء الأمريكية خطوة تنظيمية مهمة تُمهد لتسويق هذه التقنية الثورية، وطرحها الممنهج في السوق. وتوقع دوراند أن يدخل اختبار أيبايوسكوب السوق الأمريكية في العام 2018، لكنه حصل على تصريح بدخول السوق الأوروبية قبل ذلك. ووفقا للأكاديمية الأمريكية للحساسية والربو والمناعة، فقد تزايدت أمراض الحساسية العامة خلال 50 عامًا المنصرمة، نتيجة تزايد الحالات بين أطفال المدارس بنسبة 40% - 50%. وأشارت جمعية الربو والحساسية في أمريكا، إلى أن حالات الحساسية إن كانت حساسية أنفية أو حساسية ضد الأطعمة تحتل المركز السادس في أسباب الوفيات الناجمة عن الأمراض المزمنة في الولايات المتحدة. وقد يسهل التشخيص السريع لحالات الحساسية علاجها ويقلل تكلفتها، بالإضافة لإنقاذ الأرواح عبر الاكتشاف المبكر لمسببات الحساسية قبل فوات الأوان.
385
| 28 أكتوبر 2017

وافقت هيئة الغذاء والدواء الأمريكية (FDA) على أول عقار يعالج مرض "شاغاس" أو المثقبيات الأمريكي وهو مرض طفيلي ينتشر في المناطق المدارية الاستوائية. وأوضحت الهيئة في بيان تلقت الأناضول نسخة منه، اليوم الأربعاء، أن الدواء الجديد يدعى "بنزنيدازول" (Benznidazole) لعلاج الأطفال الذين تتراوح أعمارهم بين عامين و12 عامًا من مرض "شاغاس". وقال الدكتور إدوارد كوكس، مدير مكتب منتجات مضادات الميكروبات في مركز تقييم الأدوية والتابع لهيئة الغذاء والدواء الأمريكية، إن هذا الدواء هو الأول من نوعه الذي توافق عليه الهيئة لعلاج مرض "شاغاس". وأضاف أن "الهيئة تلتزم بتوفير خيارات علاجية آمنة وفعالة لعلاج الأمراض المدارية". وبحسب الهيئة، تم تجربة فاعلية وسلامة العقار عبر اثنين من التجارب السريرية التي أجريت على أطفال أعمارهم بين 6-12 عاما ومصابون بالمرض.ووجد الباحثون أن 55 إلي 60% من المرضى استجابوا للعلاج بالعقار فى التجربتين، بالمقارنة مع 14% في العلاج الوهمي. ووفقًا لمنظمة الصحة العالمية، تتراوح أعداد المصابين بمرض "شاغاس" في أنحاء العالم بين 6 إلي 7 ملايين نسمة تقريبًا، وينتشر المرض أساسًا في 21 بلداً من بلدان أمريكا اللاتينية. وأضافت أن المرض ينتقل إلى البشر في المقام الأول عن طريق الاختلاط ببراز بق "الترياتومين" الذي يُعرف بعدة أسماء منها "بق التقبيل"، بحسب المنطقة الجغرافية. ويتعرّض نحو 30% من المصابين بحالات مزمنة من "شاغاس" لاضطرابات قلبية، ويُصاب نحو 10% منهم باضطرابات هضمية أو عصبية أو اضطرابات مختلطة يتعيّن علاجها. وأُطلق اسم "شاغاس" على هذا المرض بعد قيام الطبيب البرازيلي كارلوس ريبيرو شاغاس، باكتشافه لأوّل مرّة في 1909.
1898
| 30 أغسطس 2017
وافقت هيئة الغذاء والدواء الأمريكية "FDA"، اليوم الأربعاء، على عقار جديد لعلاج المصابين بفيروس التهاب الكبد الوبائي المزمن "سي"، والذي أدّى لنسب شفاء وصلت 96 إلى 97%. وأوضحت الهيئة في بيان تلقت الأناضول نسخة منه، إن العقار الجديد يطلق عليه اسم "فوسيفي" (Vosevi) ويستخدم مرة واحدة يوميًا لعلاج فيروس "سي". وأضافت أن استخدام عقار "فوسيفي" يشمل المرضى الذين يعانون من تليف الكبد المستقر وغير المستقر، ومع جميع الأنماط الجينية للفيروس من الأول إلى السادس. ويتم استخدام العقار لمدة 8 أسابيع للمرضى الذين لا يعانون من تليف الكبد، ولمدة 12 أسبوعًا في المرضى الذين فشلت معهم العلاجات السابقة. وأشارت إلى أن هذا الدواء الجديد عبارة عن قرص دوائي مدمج من 3 مواد فعالة من مضادات الفيروسات المباشرة وهي السوفوسبوفير (sofosbuvir) والفيلباتاسفير (velpatasvir) والفوكسيلابريفير (voxilaprevir) . واختبرت الهيئة، فاعلية وسلامة العقار الجديد، على 750 من مرضى فيروس "سي" بأنماطه المختلفة من الأول إلى السادس، وبنسب تليّف كبد متفاوتة، في تجارب استمرت 12 أسبوعا. وأظهرت النتائج أن 96 إلى 97% من المرضى الذين تلقوا "فوسيفي" تعافوا من الفيروس، ولم يظهر أثره في دمائهم بعد 12 أسبوعا من الانتهاء من العلاج، ما يشير إلى أن العدوى قد انتهت. وعن آثار الدواء الجانبية، قالت الهيئة إن ردود الفعل السلبية الأكثر شيوعًا بين المرضى الذين تناولوا "فوسيفي" كانت الصداع والتعب والإسهال والغثيان.وقبل أيام، أعلنت شركة "جلياد ساينسز" الأمريكية لإنتاج الأدوية، المنتجة لعقاري "سوفالدي" و"هارفوني"، أن اللجنة العلمية لوكالة الأدوية الأوروبية (EMA)، وافقت مبدئيًا على عقار "فوسيفي" للاستخدام على نطاق تجاري. ويعتبر عقار "فوسيفي" أحدث عقار تنتجه الشركة لعلاج فيروس التهاب الكبد "سي". وفيروس "سي"، هو مرض فيروسي يمكن أن يؤدي إلى تراجع وظائف الكبد أو الفشل الكبدي، إذا لم يتم اكتشافه بسرعة، وقد ينتهي المطاف مع بعض المرضى إلى الإصابة بتليف الكبد، كما أن الفحص الفعال، والتشخيص السريع والحاسم، يوقف انتشار الفيروس. ووفق آخر إحصائيات منظمة الصحة العالمية، فإن 150 مليون مريض جديد يصابون بعدوى الفيروس سنويًا على مستوى العالم، بينهم 3.2 مليون شخص في الولايات المتحدة فقط، ويموت سنويًا أكثر من 500 ألف مريض آخرين جراء الإصابة بأمراض الكبد الناجمة عن هذا الالتهاب.
3407
| 19 يوليو 2017
وافقت هيئة الغذاء والدواء الأمريكية (FDA)، اليوم السبت، على دواء جديد لعلاج الأطفال والبالغين من مرض الخلايا المنجلية أو فقر الدم المنجلي. وأوضحت الهيئة، في بيان، أن الدواء الجديد يحمل اسم (Endari)، ويعالج المرضى الذين تتراوح أعمارهم بين 5 سنوات وكبار السن، للحد من المضاعفات الحادة المرتبطة باضطراب الدم. وأضافت أن العلاج الجديد، هو أول علاج توافق عليه لمرض فقر الدم المنجلي منذ ما يقرب من 20 عامًا، حيث لم توافق الهيئة من قبل سوى على دواء آخر للمرض. وتم دراسة سلامة وفعالية العلاج في تجربة على مجموعة من المرضى تتراوح أعمارهم بين 5 و 58 عامًا، يعانون من مرض الخلايا المنجلية. وتم تقييم تأثير العلاج على مدى 48 أسبوعا، كان المرضى الذين عولجوا بالدواء الجديد يعانون من عدد أقل من الزيارات إلى المستشفى لعلاج الألم، مقارنة بالمرضى الذين تلقوا علاجًا وهميًا. وتشمل الآثار الجانبية الشائعة للدواء الجديد الإمساك، والغثيان، والصداع، وآلام في البطن، والسعال، وآلام في الأطراف، وآلام الظهر وألم في الصدر، حسب بيان الهيئة. وهيئة الغذاء والدواء الأمريكية، هي وكالة تابعة لوزارة الولايات المتحدة لخدمات الصحة وحقوق الإنسان. و"فقر الدم المنجلي" هو أكثر أمراض فقر الدم شيوعا في العالم، ويعد من الأمراض الخطيرة التي ليس لها علاج، وعند الإصابة بالمرض لا تستمر دورة حياة كريات الدم الحمراء طويلا، مما يؤدي إلى فقر الدم وألم شديد وتلف في الأعضاء. ويحدث مرض فقر الدم المنجلي نتيجة تحور جيني يجعل كريات الدم الحمراء شاذة الشكل وقصيرة العمر، وتأخذ الكريات شكل منجل الحصاد ولذلك سُمي بالمنجلي، ويعاني المريض من فقر الدم وانسداد الأوعية الدموية وفي بعض الحالات الموت المبكر.
2432
| 08 يوليو 2017

وافقت هيئة الغذاء والدواء الأمريكية "FDA" اليوم الأربعاء، على عقار جديد لعلاج اضطراب نقص الانتباه وفرط الحركة "ADHD". وأوضحت الهيئة في بيان لها، أن العقار الجديد يدعى ستراتيرا (Strattera) لعلاج اضطراب نقص الانتباه وفرط الحركة لدى الأطفال والبالغين. وبحسب الهيئة، فإن "الآثار الجانبية الأكثر شيوعا للعقار عند الأطفال، تمثل في انخفاض الشهية، والغثيان أو القيء، والدوخة، والتعب، وتقلبات المزاج". وبالنسبة للبالغين، كانت الآثار الجانبية الأكثر شيوعًا الإمساك، وجفاف الفم والغثيان، وانخفاض الشهية، والدوخة. ويعتبر اضطراب نقص الانتباه وفرط الحركة أحد أشهر أمراض اضطراب السلوك العصبي الذي يصيب الأطفال في مرحلة الدراسة، ويتميز المصابون به بأنه لا يمكنهم التركيز أو إعطاء الاهتمام الكافي لشيء محدد. وينتج هذا الاضطراب بسبب خلل عضوي في الأجزاء التي تتحكم في الانتباه والسيطرة على النشاط في المخ، وهو الأمر الذي يجعلهم يعانون من صعوبات في تنفيذ مهام معينة، ويبدو مسلكهم غريبًا ويتصرفون باندفاع ويتعرضون لمشكلات كثيرة. وهيئة الغذاء والدواء الأمريكية، هي وكالة تابعة لوزارة الولايات المتحدة لخدمات الصحة وحقوق الإنسان، ومسؤولة عن حماية وتعزيز الصحة العامة من خلال التنظيم والإشراف على سلامة الأغذية، ومنتجات التبغ، والمكملات الغذائية، والعقاقير الطبية، والأدوية المباعة، واللقاحات، والمستحضرات الصيدلانية البيولوجية.
1471
| 31 مايو 2017

وافقت هيئة الغذاء والدواء الأمريكية "FDA" اليوم الأربعاء، على دواء جديد يستخدم كعلاج إضافي للمرضى الذين يعانون من مرض باركنسون أو الشلل الرعاش ولا يستجيبون للعلاجات الحالية. وأوضحت الهيئة في بيان، أن عقار جديد يدعى "Xadago" يستهدف بالأساس مرضى الشلل الرعاش الذي لا يستجيبون مؤقتًا لعقاري اللِّيفودوبا "Levodopa" والكاربيدوبا "Carbidopa" وهما علاجين لباركسنون، ما يسبب زيادة أعراض المرض مثل الهزة وصعوبة المشي. وتم اعتماد العقار الجديد، بعد إجراء تجربتين شملتا 1194 مريضا كانوا يتناولون عقار "ليفودوبا"، ولكنهم لم يستجيبوا لبعض الوقت للعقار. وأظهرت التجارب أن مرضى الشلل الرعاش الذين تناولوا العقار الجديد، انخفضت لديهم أعراض المرض، بالمقارنة مع مجموعة أخرى تناولت دواءً وهميًا. وأشارت الهيئة إلى أن هناك مرضى لا يجب أن يتناولوا العقار الجديد وهم الذين يعانون من مشاكل كبيرة في الكبد، أو الذين يتناولون دواء يستخدم لعلاج السعال أو البرد يسمى ديكستروميتورفان "Dextromethorphan"، أو من يتناولون دواء آخر يسمى مثبطات أكسيداز أحادي الأمين "MAOIs"، لأنه قد يسبب زيادة حادة ومفاجئة في ضغط الدم، أو أولئك الذين يتناولون العقاقير الأفيونية، كمضادات الاكتئاب لأنه قد يسبب أثر جانبي يهدد الحياة وهو متلازمة السيروتونين. وعن الآثار الجانبية الأكثر شيوعا للعقار الجديد، بينت الهيئة بأنها تمثلت في الغثيان، والأرق. والشلل الرعاش، هو أحد الأمراض العصبية، التي تصيب الأشخاص فوق 60 عامًا، وتؤدي إلى مجموعة من الأعراض أبرزها الرعاش، وبطء الحركة، بالإضافة إلى التصلب أو التخشب الذي ينتج عنه فقدان الاتزان والسقوط. ووفقا للمعاهد الوطنية الأمريكية للصحة، فإنه يتم تشخيص ما يقرب من 50 ألف حالة جديدة بمرض باركنسون سنويًا، فيما يبلغ عدد ن المصابين بالمرض مليون حالة في الولايات المتحدة.
999
| 22 مارس 2017

وافقت هيئة الغذاء والدواء الأمريكية "FDA" على دواء جديد، لعلاج حساسية عث الغبار المنزلي، التي قد ينجم عنها حساسية الأنف والتهاب العين، ويُسمح للمرضى الذين تتراوح أعمارهم بين 18 إلى 65 عامًا، فقط بتناول هذا الدواء. وأوضحت الهيئة، في بيان لها، اليوم الخميس، أن الدواء الجديد يسمى "Odactra" ويعمل على تدريب وتهيئة الجهاز المناعي، للحد من شدة أعراض حساسية عث الغبار المنزلي. وبينت الهيئة أنها وافقت على الدواء الجديد، بعد تجربته في الولايات المتحدة وكندا وأوروبا، على ما يقرب من 2500 شخص مصابون بحساسية عث الغبار المنزلي، تلقى نصفهم دواء "Odactra" بينما تلقى النصف الآخر حبوب وهمية. ووجد الباحثون، أن المرضى الذين تلقوا الدواء الجديد انخفضت لديهم أعراض الحساسية، كما انخفضت لديهم الحاجة إلى اللجوء لأدوية أخرى لتخفيف أعراض الحساسية، بالمقارنة مع من تلقوا دواءً وهميًا. وعن الأعراض الجانبية الأكثر شيوعًا للدواء، أفادت الهيئة بأنها تمثلت في الغثيان، وحكة في الأذنين والفم، وتورم في الشفتين واللسان. وتنجم حساسية عث الغبار المنزلي عن تواجد حشرة العث المنزلي، التي تنتمي لعائلة العنكبوتيات، وهي كائنات غير مرئية بالعين المجردة، تعيش على مدار العام في المنازل، وتسكن الفراش، الأغطية، السجاد، والستائر.
1563
| 02 مارس 2017

أجازت هيئة الغذاء والدواء الأمريكية "FDA" أول عقار لعلاج الأطفال والبالغين الذين يعانون من ضمور العضلات الشوكي، وهو مرض وراثي نادر، غالبًا ما يكون مميتًا، يؤثر على قوة العضلات والحركة. وأوضحت الهيئة في بيان لها، اليوم السبت، أن العقار الجديد يطلق عليه اسم "Spinraza"، وهو عبارة عن حقن تؤخذ في المنطقة المحيطة بالحبل الشوكي، مضيفة "كان هناك حاجة منذ فترة طويلة لعلاج لضمور العضلات الشوكي، وهو السبب الجيني الأكثر شيوعًا للوفاة بين الرضع، وأحد الأمراض التي يمكن أن تؤثر على الناس في أي مرحلة من مراحل حياتهم". وأوضحت أن "الموافقة على العقار جاءت بعد إجراء تجارب على 121 طفلًا يعانون من ضمور العضلات الشوكي، وتم تشخيص إصابتهم بالمرض قبل بلوغهم 6 أشهر من العمر"، وأثبتت النتائج أن 40% من المرضى الذين تلقوا العلاج شهدوا تحسنًا في المراحل الحركية، مثل التحكم في الرأس، والجلوس، والزحف والوقوف والمشي، بالمقارنة مع مجموعة أخرى تلقت دواءً وهميًا. وكانت الآثار الجانبية الأكثر شيوعًا للعقار الجديد، وفقًا للهيئة، هي التهابات الجهاز التنفسي والإمساك. وضمور العضلات الشوكي، مرض وراثي يصيب الأعصاب التي تظهر من الحبل الشوكي الموجود في العمود الفقري، ويظهر على شكل ضمور عضلات الأطراف مع ارتخاء شديد وضعف في العضلات، وهذا يعني أن لدى الأشخاص المصابين بالمرض مشاكل في التنفّس والبلع.
5184
| 24 ديسمبر 2016

وافقت هيئة الغذاء والدواء الأمريكية "FDA"، على دواء جديد يحسّن حياة مرضى السكري من النوع الثاني، ويحد من موتهم بأمراض القلب والأوعية الدموية. وأوضحت الهيئة في بيان لها أمس السبت، أن الدواء الجديد يدعى "Jardiance"، كانت اعتمدته "FDA" في 2014، كدواء لتحسين السيطرة على نسبة السكر في الدم لدى مرضى السكري. وبحسب الهيئة، فإن أمراض القلب والأوعية الدموية تعد سببًا رئيسيًا لوفاة البالغين المصابين بالنوع الثاني من مرض السكري. وتم اعتماد الدواء، بعد إجراء تجارب سريرية على أكثر من 7000 مريض يعانون من النوع الثاني من مرض السكري، وأمراض القلب والأوعية الدموية. وأثبتت النتائج، أن الدواء يحد من خطر الموت بأمراض القلب والأوعية الدموية، مقارنة مع الدواء الوهمي. وكشفت الهيئة أن الآثار الجانبية الأكثر شيوعا لدواء "Jardiance" هي التهابات المسالك البولية والتهابات الأعضاء التناسلية للإناث. ووفقا لمنظمة الصحة العالمية، فإن حوالي 90% من الحالات المسجلة في شتى أرجاء العالم لمرض السكري، هي حالات من النوع الثاني، الذي يظهر أساساً جرّاء فرط الوزن وقلّة النشاط البدني، ومع مرور الوقت، يمكن للمستويات المرتفعة من السكر في الدم، أن تزيد من خطر الإصابة بأمراض القلب، والعمى، والأعصاب والفشل الكلوي.
394
| 04 ديسمبر 2016

وافقت هيئة الغذاء والدواء الأمريكية "FDA" على دواء جديد لعلاج مرضى السكري من النوع الثاني، جنبًا إلى جنب مع إتباع نظام غذائي وممارسة التمارين الرياضية. وأوضحت الهيئة، في بيان لها اليوم الخميس، أن الدواء الجديد الذي يحمل اسم "Adlyxin" عبارة عن حقنة واحدة تؤخذ يوميًا، تضبط مستويات السكر في الدم. موافقة الهيئة على الدواء الجديد، جاءت بعد تقييم سلامته وفعاليته، في 10 تجارب سريرية، أجريت على 5 آلاف و400 من المرضى الذين يعانون من السكري من النوع الثاني. وأثبتت التجارب أن الدواء يضبط مستويات السكر في الدم، حتى مع المرضى المعرضين لخطر أمراض القلب والأوعية الدموية، لكنها نصحت مرضى السكري من النوع الأول بعدم تناول الدواء الجديد. ووفقا لمنظمة الصحة العالمية، فإن حوالي 90% من حالات السكري المسجّلة في شتى أرجاء العالم هي حالات من النوع الثاني، الذي يظهر أساساً جرّاء فرط الوزن وقلّة النشاط البدني، ومع مرور الوقت، يمكن للمستويات المرتفعة من السكر في الدم، أن تزيد من خطر الإصابة بأمراض القلب، والعمى، والأعصاب والفشل الكلوي. في المقابل، تحدث الإصابة بالنوع الأول من السكر عند قيام النظام المناعي في الجسم بتدمير الخلايا التي تتحكم في مستويات السكر في الدم. وأشارت المنظمة إلى أن 422 مليون شخص حول العالم مصابون بمرض بالسكري، ويبلغ نصيب إقليم شرقِ المتوسطِ منهم 43 مليون شخص.
456
| 28 يوليو 2016

وافقت هيئة الغذاء والدواء الأمريكية "FDA" على لقاح جديد لوقاية البالغين من مرض الكوليرا، قبل السفر إلى المناطق الموبوءة بالمرض، بعد أن بلغت فاعليته 90%. وقالت الهيئة في بيان لها، اليوم السبت، إن اللقاح الجديد يسمى "Vaxchora"، ويعتبر الوحيد الذي اعتمدته الهيئة الأمريكية للوقاية من المرض، مضيفة أن اللقاح يقي البالغين الذين تتراوح أعمارهم بين 18 و 64 عاما، من السلالة التي تسمى "المصلية O1" المسببة للكوليرا. وأشارت الهيئة، إلى أن اللقاح الجديد يؤخذ مرة واحدة فقط عن طرق الفم، قبل 10 أيام على الأقل، من السفر إلى المناطق المتضررة من المرض. واعتمدت الهيئة اللقاح بعد أن أثبت فاعليته، في التجارب التي أجريت على 197 متطوعًا في الولايات المتحدة الأمريكية، تتراوح أعمارهم بين 18 إلى 45 عامًا، وسبق ذلك تجارب سريرية أجريت على 3 آلاف و235 شخصًا.
610
| 11 يونيو 2016

وافقت هيئة الغذاء والدواء الأمريكية (FDA) على طرح عقار جديد لعلاج "سرطان المثانة البولية"، يستهدف المرضى الذين يعانون من المرض في مراحله المتقدمة. وقالت الهيئة، في بيان نشرته على موقعها الإلكتروني، إن "العقار الجديد الذي يحمل اسم (Tecentriq)، يتميز بأنه ينتمي لفئة الأدوية الموجهة، أي أنه يستهدف الخلايا السرطانية فقط، دون التأثير على الخلايا الصحيحة، إلا بنسبة قليلة". وبحسب الهيئة، فإن الدواء الجديد يحتوى على المادة الفعالة (atezolizumab)، وهو مخصص لعلاج أكثر أنواع "أورام المثانة" شيوعا، ويعرف باسم "سرطان المثانة البولية السطحي"، أي أن الورم يصيب "الخلايا المبطنة للمثانة"، ولا يؤثر على العضلات الداخلية الخاصة بها. ويعمل العقار عن طريق تثبيط بعض البروتينات الموجود في خلايا الجهاز المناعي للجسم وخلايا الأورام، وهو ما يساعد في النهاية الجهاز على مكافحة الخلايا السرطانية، والحد من حجم الورم، كما تقول هيئة الغذاء والدواء الأمريكية. ووافقت الهيئة على العقار الجديد، بعد تجارب أجريت على 310 من المرضى بسرطان المثانة البولية، لمدة 14 شهرا، وكانت النتائج جيدة، حيث حدث انكماش في حجم الأورام بنسب متوسطة. وعن أبرز الآثار الجانبية للعقار، أفادت الهيئة في بيانها، بأن المرضى الذي يتناولون العقار، قد يشعرون بالإعياء، وانخفاض الشهية، والغثيان، وعدوى الجهاز البولي، والحمى، والإمساك. وتشير الأبحاث، إلى أنه يتم تشخيصها ما يقرب من 76 ألف حالة جديدة لـ"سرطان المثانة" سنويا، في الولايات المتحدث الأمريكية وحدها، ويتطور المرض لدى الرجال حوالي 3 إلى 4 مرات أكثر من النساء، ويصيب غالبا لكبار السن.
1499
| 21 مايو 2016

اعتمدت هيئة الغذاء والدواء الأمريكية "FDA"، دواء جديدا لعلاج المرضى الذين يعانون من سرطان الدم الليمفاوي المزمن، حسبما أوضحت الهيئة في بيان لها، مساء اليوم الإثنين. ووافقت الهيئة على الدواء الجديد، الذي يسمى "Venclexta"، ويستهدف خلايا سرطان الدم الليمفاوي المزمن بعد إجراء تجارب سريرية على 106 من مرضى سرطان الدم الليمفاوي المزمن، الذين تلقوا العلاج على مدى 5 أسابيع بجرعات مختلفة. والنتائج أظهرت أن 80% من المشاركين في التجارب تعافوا كليًا أو جزئيًا من سرطان الدم الليمفاوي المزمن. وتمثلت الآثار الجانبية الأكثر شيوعا للدواء الجديد في انخفاض عدد خلايا الدم البيضاء، والإسهال، والغثيان، وفقر الدم، وعدوى الجهاز التنفسي العلوي، وانخفاض عدد الصفائح الدموية والتعب. ووفقا للمعهد القومي للسرطان بأمريكا، فإن سرطان الدم الليمفاوي المزمن هو أحد أكثر أنواع سرطانات الدم شيوعًا بين البالغين، ويصيب ما يقرب من 15 ألف شخص جديد سنويًا في أمريكا وحدها.
1209
| 11 أبريل 2016
وافقت هيئة الغذاء والدواء الأمريكية "FDA"، على عقار جديد، لعلاج الأشخاص، الذين يصابون بسرطان الرئة في مراحله المتقدمة، ولا يستطيعون تحمل العلاجات المتاحة للمرض حاليًا. وأوضحت الهيئة، في بيان لها اليوم السبت، أن العقار الجديد يحمل اسم أليسنسا "Alecensa"، ويستهدف المرضى الذين يعانون من سرطان خلايا الرئة غير الصغيرة، هو النوع الأكثر شيوعًا من سرطان الرئة، ولا يستجيبون لعلاج آخر للمرض، يسمى "Xalkori". وقالت الهيئة، إن موافقتها على العلاج الجديد توفر خيارًا أفضل لمرضى سرطان الرئة، الذي وصل فيه المرض إلى مرحلة خطيرة للغاية، وأصبح ينتقل من الرئة إلى أجزاء الجزء الجسم الأخرى. وتمت الموافقة على العقار الجديد، بعد اختبار سلامته وفاعليته، من خلال تجربتين سريريتين، استمرتا حوالي عام، ووجد الباحثون أن العقار الجديد الذي يؤخذ عن طريق الفم، مرتين يوميًا، يوقف نمو وانتشار سرطان خلايا الرئة. وقالت الهيئة إن "الآثار الجانبية الأكثر شيوعًا للعقار الجديد، تتمثل في التعب، والإمساك، وآلام في العضلات".
1217
| 12 ديسمبر 2015

أعلنت هيئة الغذاء والدواء الأمريكية "FDA"، عن دواء جديد لعلاج فيروس نقص المناعة البشرية الإيدزعند الأطفال والكبار، اليوم الجمعة، ويحمل اسم "جينفويا" (Genvoya)، وهو بمثابة أقراص دواء متكاملة، تعالج عدوى فيروس الإيدز عند الأطفال البالغين من العمر 12 عامًا، بالإضافة إلى الكبار. وقال مدير مكتب هيئة الغذاء والدواء الأمريكية للمنتجات المقاومة للميكروبات، الدكتور إدوارد كوكس، أن العقاقير الجديد عبارة عن كبسولات تؤخذ مرة واحدة يوميًا، وتحتوي على شكل جديد من مادة تينوفوفير (Tenofovir) المضادة للطفيليات. وأكدت الهيئة إنه تم تقييم سلامة وفعالية العلاج الجديد، من خلال تجربته على 3171 مشاركًا في 4 تجارب سريرية، وأظهرت النتائج سلامته وفاعليته في الحد من الأحمال الفيروسية لمرض الإيدز، فيما تشمل الآثار الجانبية الأكثر شيوعًا للدواء الجديد الغثيان، ولا ينصح بتناول مرضى قصور الكلوي الحاد الدواء الجديد.
13293
| 06 نوفمبر 2015
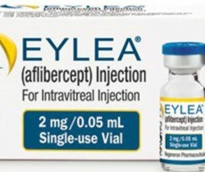
وافقت هيئة الغذاء والدواء الأمريكية (FDA)، على علاج جديد، لمرض اعتلال الشبكية السكرى، هو أحد الأسباب الرئيسية المؤدية إلي العمى، لدى الأشخاص المصابين بمرض السكرى، من النوع الأول والثاني الذين تتراوح أعمارهم بين 20 إلى 47 عامًا. وأوضحت الهيئة فى بيان اليوم الخميس، أن العلاج الجديد عبارة عن حقن تحمل اسم (Eylea)، وتحقن داخل عين المريض لعلاج اعتلال الشبكية السكري، وهو أحد مضاعفات مرض السكري، التي يمكن أن تؤدي في النهاية إلى العمى. وأضافت الهيئة أن العلاج أثبت فاعليته وأمانه، بعد خضوع 679 شخصًا لاثنين من التجارب السريرية، وكانت النتائج إيجابية للغاية، حيث ساهم الدواء في علاج أعراض مرض اعتلال الشبكية السكرى. وعن الجرعة الموصى بها من العلاج الجديد، نصحت الهيئة الطبيب المختص بحقن (Eylea) داخل عين المريض بمعدل مرة واحدة شهريًا، لمدة 5 أشهر، بعدها يتم تغيير إستراتيجية العلاج، ليتم حقن المريض بمعدل حقنة كل شهرين، على أن يتم ضبط مستويات السكر والكولسترول والضغط الخاصة بالمريض أثناء حصوله على العقار. لكن الهيئة أشارت إلى أن أبرز الآثار الجانبية للعلاج، التي حدثت لبعض المرضى، تمثلت في حدوث نزيف في ملتحمة العين، وآلام في العين وارتفاع ضغط العين.
1033
| 26 مارس 2015
مساحة إعلانية
الأكثر مشاهدة

أعلن محمد الشبرمي مدير الهيئة الخليجية للسكك الحديدية عن اكتمال تنفيذ 50% من مشروع سكة الحديد الرابطة بين دول الخليج، والتي يمتد طولها...
27746
| 11 مايو 2026

• افتتاح 9 رياض أطفال العام المقبل نظراً للإقبال المتزايد على مرحلة ما قبل الروضة • خدمة إلكترونية عبر معارف للتسجيل بالمراكز المسائية...
18588
| 10 مايو 2026

شهد طريق أم باب، الرابط بين مدينة دخان وشارع سلوى، قبل أيام، حادثاً مأساوياً أعاد إلى الواجهة مطالبات قديمة وأخرى متجددة بضرورة تطوير...
12470
| 12 مايو 2026

حمل تطبيق الشرق
تابع الأخبار المحلية والعالمية من خلال تطبيقات الجوال المتاحة على متجر جوجل ومتجر آبل
الأكثر رواجاً
- 1 الشرق تنشر جدول اختبارات نهاية الفصل الدراسي الثاني
أعلنت وزارة التربية والتعليم والتعليم العالي، اليوم، عن بدء اختبارات منتصف الفصل الدراسي الثاني للعام الدراسي 2025–2026 للصفوف من الأول وحتى الثاني عشر،...
7844
| 11 مايو 2026
- 2 طولها يساوي ربع محيط الأرض.. بالأرقام: قطر توفر شبكة مياه عالية الكفاءة وأكبر خزانات استراتيجية في العالم
400 مليون جالون متوسط الاحتياج اليومي من المياه 15 خزان مياه استراتيجياً الأكبر على مستوى العالم كهرماء تمتلك أنبوباً للمياه يكفي لعبور سيارة...
6714
| 12 مايو 2026
- 3 وزارة الدفاع القطرية تعلن عن تعرض سفينة بضائع لاستهداف بطائرة مسيّرة
أعلنت وزارة الدفاع القطرية عن تعرض سفينة بضائع تجارية في المياه الإقليمية للدولة، شمال شرق ميناء مسيعيد، قادمة من أبو ظبي، صباح اليوم...
5392
| 10 مايو 2026



